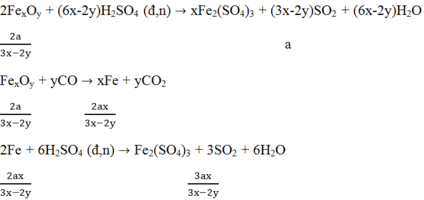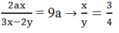Gỉa sử lấy V ml đ HCl 36,5% (D=1,2g/mol) để hòa tan hoàn toàn 53,55 g oxit Kl (R2On) chứa 89,54% KL. Tìm V

Những câu hỏi liên quan
Bài 1: Khử 13,38(g) 1 oxit của KL + hết 1,344(l) H2 (đktc).xđ KLBài 2: Hòa tan hoàn toàn 8,9 g h2 2 kL : A,B có cùng hóa trị II và có tỉ lệ mol là 1: 1 d2 HCL thu đc 4,48(l) H2(đktc) .Hỏi A,B là KL nào trong số các KL sau : Mg,Ca,Ba,Fe,2nBài 3 : Để hòa tan 9,6 g 1 h2 đồng mol 2 oxit có hóa trị III cần 14,6g HCL xđct của 2 oxit trên biết KL hóa trị II có thể là (Be,Mg,Ca,2n)Bài 4: Hòa tan hoàn toàn 3,78g 1KL A d2 HCL - 4,704 (L) H2(đktc) . xđ KL A (Al)
Đọc tiếp
Bài 1: Khử 13,38(g) 1 oxit của KL + hết 1,344(l) H2 (đktc).xđ KL
Bài 2: Hòa tan hoàn toàn 8,9 g h2 2 kL : A,B có cùng hóa trị II và có tỉ lệ mol là 1: 1 = d2 HCL thu đc 4,48(l) H2(đktc) .Hỏi A,B là KL nào trong số các KL sau : Mg,Ca,Ba,Fe,2n
Bài 3 : Để hòa tan 9,6 g 1 h2 đồng mol 2 oxit có hóa trị III cần 14,6g HCL xđct của 2 oxit trên biết KL hóa trị II có thể là (Be,Mg,Ca,2n)
Bài 4: Hòa tan hoàn toàn 3,78g 1KL A= d2 HCL -> 4,704 (L) H2(đktc) . xđ KL A (Al)
Bài 1 . Gọi CT của oxit là R2On (n là hóa trị của R)
\(R_2O_n+nH_2\rightarrow2R+nH_2O\)
0,06/n<-----0,08
=> \(\dfrac{13,38}{2R+16n}=\dfrac{0,06}{n}\)
n=1 => R=103,5 (loại)
n=2 => R=207 (Pb)
n=3 => R=310,5 (loại)
Vậy kim loại cần tìm là Pb
Đúng 1
Bình luận (0)
2. \(A+2HCl\rightarrow ACl_2+H_2\)
\(B+2HCl\rightarrow BCl_2+H_2\)
Ta có : \(n_A=n_B=\dfrac{1}{2}\Sigma n_{H_2}=0,1\left(mol\right)\)
Ta có : \(0,1.M_A+0,1.M_B=8,9\)
=> \(M_A+M_B=89\)
Xét bảng sau:
| A | 24 | 40 | 56 | 137 |
| B | 65 | 49 | 33 | / |
Vậy A là Mg và B là Zn
Đúng 1
Bình luận (0)
Bài 3 :
Gọi hai oxit là XO, YO
Gọi số mol XO là a → số mol YO là a
→ mhh = a · (X +16) + a · (Y + 16) = 9,6 (gam) (1)
PTHH:
XO + 2HCl → XCl2 + H2O
YO + 2HCl → YCl2 + H2O
Theo PTHH: \(n_{HCl}=2n_{XO}+2n_{YO}=0,4\left(mol\right)\)
=> \(2a+2a=0,4\Rightarrow a=0,1\left(mol\right)\)
Thay a=0,1 (mol) vào (1) => \(X+16+Y+16=96\)
=> \(X+Y=64\)
Vì 2 kim loại có thể là Be,Mg,Ca,2n
=> Chỉ có 2 kim loại Mg, Ca thỏa mãn
Đúng 1
Bình luận (0)
Xem thêm câu trả lời
Hòa tan hoàn toàn một lượng hỗn hợp Na và K vào nước được dung dịch A và V lít khí ở đktc. Để trung hòa hòa toàn dung dịch A phải dùng 75 ml dung dịch H2SO4 0,5M. Vậy V có giá trị là:
A. 0,56 lít
B. 0,672 lít
C. 0,84 lít
D. 1,12 lít
Đáp án C
Bài toán này có thể giải ngắn gọn như sau:
Số mol tạo ra = số mol H+ trung hòa = 2. Số mol H2
⇒ Số mol H2 = 0,075 : 2 = 0,00375 ⇒ V = 0,84 lít
Đúng 0
Bình luận (0)
hỗn hợp M gồm 2 kim loại A và B có hóa trị không đổi. Oxit hõa hoàn toàn 6,3 gam M trong O2 dư thu 11,1 g hỗn hợp 2 oxit. Mặt khãc nếu lấy 12,6 gam M hòa tan hết trong dung dịch HCl. thu được V lít khí H2 Tìm V
Ầy ! Học tốt nha ^-^
- Xét thí nghiệm 1 : mO2 (ĐLBTKL) = 11.1-6.3=4.8 (g)
=> nO2=0.15(mol)
=> O2 + 4e\(\rightarrow\) 2O2- => ne (nhận ) = 0.15 x 4 = 0.6 (mol)
- Do A,B hóa trị không đổi + các phản ứng xảy ra hoàn toàn => e(nhận) tn2 = e(nhận) tn1 =0.6 mol
2H+ + 2e\(\rightarrow\) H2 => nH2 = 0.6/2=0.3 mol
=> V H2 = 6.72 l
45. Khử hoàn toàn 7,12 gam oxit kim loại bằng khí hiđro dư, sau khi phản ứng kết thúc thu được 1,602 gam nước. Nếu hòa tan hết lượng oxit trên vào dd HCl thì nhận được 0,089 mol muối clorua.a/Tìm công thức oxit b/Tính khối lượng chất rắn thu được sau khi khửc/Tính thể tích dd HCl 1,2M cần dùng.
Đọc tiếp
45. Khử hoàn toàn 7,12 gam oxit kim loại bằng khí hiđro dư, sau khi phản ứng kết thúc thu được 1,602 gam nước. Nếu hòa tan hết lượng oxit trên vào dd HCl thì nhận được 0,089 mol muối clorua.
a/Tìm công thức oxit b/Tính khối lượng chất rắn thu được sau khi khử
c/Tính thể tích dd HCl 1,2M cần dùng.
Hòa tan hoàn toàn m gam Fe bằng dung dịch HNO3 thu được dung dịch X và 1,12 lít NO (đktc). Thêm dung dịch chứa 0,1 mol HCl vào dung dịch X thì thấy khí NO tiếp tục thoát ra và thu được dung dịch Y. Để phản ứng hết với các chất trong dung dịch Y cần 115 ml dung dịch NaOH 2M. Giá trị của m là A. 3,36 B. 4,2 C. 3,92 D. 3,08
Đọc tiếp
Hòa tan hoàn toàn m gam Fe bằng dung dịch HNO3 thu được dung dịch X và 1,12 lít NO (đktc). Thêm dung dịch chứa 0,1 mol HCl vào dung dịch X thì thấy khí NO tiếp tục thoát ra và thu được dung dịch Y. Để phản ứng hết với các chất trong dung dịch Y cần 115 ml dung dịch NaOH 2M. Giá trị của m là
A. 3,36
B. 4,2
C. 3,92
D. 3,08
Đáp án : C
Fe được hòa tan hoàn toàn bởi dd HNO3 thu được dd X, khi thêm HCl vào X có khí NO thoát ra → trong X có ion Fe2+ → HNO3 đã phản ứng hết
n(NO) = 1,12/22,4 = 0,05 mol
Fe + 4HNO3 → Fe(NO3)3 + NO + 4H2O
0,05 -> 0,2 -> 0,05
Fe + 2Fe(NO3)3 → 3Fe(NO3)2
x -> 3x
Theo ĐL bảo toàn nguyên tố, số mol NO3- có trong muối:
n(NO3- trong muối) = n(HNO3) - n(NO) = 0,15 mol
n(NaOH) = 0,115.2 = 0,23 mol
Sau khi NaOH pư hoàn toàn với các chất trong dd Y, dung dịch thu được có:
n(Na+) = n(NaOH) = 0,23 mol; n(Cl-) = n(HCl) = 0,1 mol → n(NO3-) = n(Na+) - n(Cl-) = 0,23 - 0,1 = 0,13 mol → Số mol NO3- bị Fe2+ khử: 0,15 - 0,13 = 0,02 mol
NO3- + 3Fe2+ + 4H+ → 3Fe3+ + NO + 2H2O
0,02 -> 0,06 -> 0,08
NO3- và H+ đều dư (H+ dư 0,02mol) → Fe2+ đã phản ứng hết
→ 3x = 0,06 → x = 0,02 mol
Tổng số mol Fe: n(Fe) = 0,05 + x = 0,07 mol
Khối lượng Fe đã sử dụng: m(Fe) = 0,07.56 = 3,92g
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 7,6g A (kim loại nhóm IIA và oxit của nó) bằng 100ml dung dịch HCl thu được 3,36l khí (đktc) và dung dịch B chứa 0,25mol muối
a/ Viết ptpư, tìm kim loại trên
b/ Cho toàn bộ đung dịch B tác dụng vừa đủ vơí Đung dịch AgNO3 thu được 86,1g kết tủa. Tính nồng độ mol dung dịch HCl đã dùng.
Mong các bạn giúp mình, mình đang cần gấp
Đọc tiếp
Hòa tan hoàn toàn 7,6g A (kim loại nhóm IIA và oxit của nó) bằng 100ml dung dịch HCl thu được 3,36l khí (đktc) và dung dịch B chứa 0,25mol muối
a/ Viết ptpư, tìm kim loại trên
b/ Cho toàn bộ đung dịch B tác dụng vừa đủ vơí Đung dịch AgNO3 thu được 86,1g kết tủa. Tính nồng độ mol dung dịch HCl đã dùng.
Mong các bạn giúp mình, mình đang cần gấp
1) Hòa tan hoàn toàn 2,81g h2 gồm Fe2O3, MgO, ZnO trong 500ml dd H2SO4, 0,1M (vừa đủ). Sau pư, h2 muối sunphat khan thu được khi cô cạn dd đó có KL là bao nhiêu gam
2) Hòa tan hoàn toàn 16g oxit kim loại M cần dùng 600ml dd HCl 1M. Xác định CTHH của oxit kim loại
3)Hòa tan hoàn toàn 12,1g h2 bột CuO và ZnO cần dùng 100ml dd HCl 3M. Biết H100% a) Tính TP % theo khối lượng hỗn hợp ban đầu b)T...
Đọc tiếp
1) Hòa tan hoàn toàn 2,81g h2 gồm Fe2O3, MgO, ZnO trong 500ml dd H2SO4, 0,1M (vừa đủ). Sau pư, h2 muối sunphat khan thu được khi cô cạn dd đó có KL là bao nhiêu gam
2) Hòa tan hoàn toàn 16g oxit kim loại M cần dùng 600ml dd HCl 1M. Xác định CTHH của oxit kim loại
3)Hòa tan hoàn toàn 12,1g h2 bột CuO và ZnO cần dùng 100ml dd HCl 3M. Biết H=100% a) Tính TP % theo khối lượng hỗn hợp ban đầu b)Tính nồng độ mol/lít của dd sau pư c) Tính m dd H2SO4 loãng 20% cần dùng để hòa tan hỗn hợp nói trên
4) hòa tan 8,8g Mg, MgO bằng 1 lượng dd HCl 14,6% vừa đủ. Cô cạn dd thu được 28,5g muối khan a) Tính TP % theo m mỗi chất trong h2 đầu b) tính m dd HCl cần lấy c) Tính C% muối tạo thành trong dd sau pư
Bài 1:
\(n_{H_2SO_4}=0,1.0,5=0,05\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4}=0,05.98=4,9\left(g\right)\)
\(\Rightarrow n_H=2.n_{H_2SO_4}=2.0,05=0,1\left(mol\right)\)
\(\Rightarrow n_{H_2O}=\frac{n_H}{2}=\frac{0,1}{2}=0,05\left(mol\right)\)
\(\Rightarrow m_{H_2O}=0,05.18=0,9\left(g\right)\)
Theo định luật bảo toàn khối lượng ta có:
\(m_{muoi}=m_{hhđ}+m_{H_2SO_4}-m_{H_2O}=2,81+4,9-0,9=6,81\left(g\right)\)
Đúng 0
Bình luận (0)
Bài 2/ Gọi CTHH của oxit M là M2Ox
\(M_2O_x\left(\frac{0,3}{x}\right)+2xHCl\left(0,6\right)\rightarrow2MCl_x+xH_2O\)
\(n_{HCl}=1.0,6=0,6\left(mol\right)\)
\(\Rightarrow m_{M_2O_x}=\frac{0,3}{x}.\left(2M+16x\right)=16\)
\(\Leftrightarrow M=\frac{56x}{3}\)
Thế x = 1, 2, 3, ... ta nhận x = 3, M = 56
Vậy công thức oxit đó là: Fe2O3
Đúng 0
Bình luận (0)
Bài 3:
a/ Gọi số mol của CuO, ZnO lần lược là x, y
\(CuO\left(x\right)+2HCl\left(2x\right)\rightarrow CuCl_2\left(x\right)+H_2O\)
\(ZnO\left(y\right)+2HCl\left(2y\right)\rightarrow ZnCl_2\left(y\right)+H_2O\)
Ta có: \(80x+81y=12,1\left(1\right)\)
\(n_{HCl}=0,1.3=0,3\left(mol\right)\)
\(\Rightarrow2x+2y=0,3\left(2\right)\)
Từ (1) và (2) ta có hệ: \(\left\{\begin{matrix}80x+81y=12,1\\2x+2y=0,3\end{matrix}\right.\)
\(\Leftrightarrow\left\{\begin{matrix}x=0,05\\y=0,1\end{matrix}\right.\)
\(\Rightarrow m_{CuO}=0,05.80=4\left(g\right)\)
\(\Rightarrow\%CuO=\frac{4}{12,1}.100\%=33,06\%\)
\(\Rightarrow\%ZnO=100\%-33,06\%=66,94\%\)
b/ \(C_M\left(MgCl_2\right)=\frac{0,05}{0,1}=0,5\left(M\right)\)
\(C_M\left(ZnO\right)=\frac{0,1}{0,1}=1\left(M\right)\)
c/ \(MgO\left(0,05\right)+H_2SO_4\left(0,05\right)\rightarrow MgSO_4+H_2O\)
\(ZnO\left(0,1\right)+H_2SO_4\left(0,1\right)\rightarrow ZnSO_4+H_2O\)
\(\Rightarrow n_{H_2SO_4}=0,05+0,1=0,15\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4}=0,15.98=14,7\left(g\right)\)
\(\Rightarrow m_{ddH_2SO_4}=\frac{14,7}{20\%}=73,5\left(g\right)\)
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Hòa tan hoàn toàn m (g) một oxit sắt bằng H2SO4 đặc nóng thu được a mol SO2 (duy nhất). Mặt khác, sau khi khử hoàn toàn m (g) oxit trên bằng H2 ở nhiệt độ cao rồi cho toàn bộ lượng sắt tạo thành vào H2SO4 đặc nóng dư thì thu được 9a mol SO2 (duy nhất). Vậy oxit sắt là: A. FeO B. Fe2O3 C. Fe3O4 D. FeO hoặc Fe2O3
Đọc tiếp
Hòa tan hoàn toàn m (g) một oxit sắt bằng H2SO4 đặc nóng thu được a mol SO2 (duy nhất). Mặt khác, sau khi khử hoàn toàn m (g) oxit trên bằng H2 ở nhiệt độ cao rồi cho toàn bộ lượng sắt tạo thành vào H2SO4 đặc nóng dư thì thu được 9a mol SO2 (duy nhất). Vậy oxit sắt là:
A. FeO
B. Fe2O3
C. Fe3O4
D. FeO hoặc Fe2O3
Hòa tan hoàn toàn 39,7g hỗn hợp gồm BaCO3 và CaCO3 vào dung dịch H2SO4 20%, sau phản ứng thu được 6,72l khí CO2 ở đktc
a) Tính số mol khí CO2
b)Tính KL mỗi muối có trong hỗn hợp ban đầu
c) Tính % KL mỗi muối trong hỗn hợp ban đầu
d) Tính KL dung dịch axit cần dùng
(H=1; S=32; Ca=40; O=16; C=12; Ba=137)
BaCO3 + H2SO4 -> BaSO4 + CO2 + H2O (1)
CaCO3 + H2SO4 -> CaSO4 + CO2 + H2O (1)
nCO2=0,3(mol)
Đặt nBaCO3=a
nCaCO3=b
Ta có:
\(\left\{{}\begin{matrix}197a+100b=39,7\\a+b=0,3\end{matrix}\right.\)
=>a=0,1;b=0,2
mBaCO3=197.0,1=19,7(g)
mCaCO3=100.0,2=20(g)
%mBaCO3=\(\dfrac{19,7}{39,7}.100\%=49,622\%\)
%mCaCO3=100-49,622=50,378%
d;
Theo PTHH 1 và 2 ta có:
nBaCO3=nH2SO4(1)=0,1(mol)
nCaCO3=nH2SO4(2)=0,2(mol)
mH2SO4=98.0,3=29,4(g)
mdd =29,4:20%=147(g)
Đúng 0
Bình luận (0)